활성탄(AC)은 목재, 코코넛 껍질, 석탄, 솔방울 등으로부터 생산되는 높은 다공성과 흡착 능력을 지닌 고탄소성 물질을 말합니다. AC는 다양한 산업 분야에서 물과 대기 중 여러 오염 물질을 제거하는 데 널리 사용되는 흡착제 중 하나입니다. 농업 폐기물로부터 합성되는 AC는 기존에 사용되던 비재생성 고가 원료를 대체할 수 있는 훌륭한 대안으로 주목받고 있습니다. AC 제조에는 탄화와 활성화라는 두 가지 기본 공정이 사용됩니다. 첫 번째 공정에서는 원료 물질을 400~850°C의 고온에 노출시켜 휘발성 성분을 제거합니다. 고온은 수소, 산소, 질소와 같은 비탄소 성분을 기체 및 타르 형태로 제거합니다. 이 공정을 통해 탄소 함량은 높지만 표면적과 다공성이 낮은 숯이 생성됩니다. 두 번째 단계는 이렇게 합성된 숯을 활성화하는 과정입니다. 활성화 과정 중 모공 크기 증가는 크게 세 가지로 분류할 수 있습니다. 기존에 접근할 수 없었던 모공의 개방, 선택적 활성화를 통한 새로운 모공 생성, 그리고 기존 모공의 확장입니다.
일반적으로 원하는 표면적과 다공성을 얻기 위해 물리적 활성화와 화학적 활성화라는 두 가지 접근 방식이 사용됩니다. 물리적 활성화는 고온(650~900°C)에서 공기, 이산화탄소, 수증기와 같은 산화성 기체를 사용하여 탄화된 숯을 활성화하는 것입니다. 이산화탄소는 순수한 성질, 손쉬운 취급, 그리고 약 800°C에서 제어 가능한 활성화 공정 때문에 일반적으로 선호됩니다. 이산화탄소 활성화는 수증기 활성화에 비해 높은 기공 균일성을 얻을 수 있습니다. 그러나 물리적 활성화에서는 상대적으로 높은 표면적을 가진 활성탄을 생산할 수 있기 때문에 이산화탄소보다 수증기가 훨씬 더 선호됩니다. 물 분자의 크기가 작기 때문에 숯 구조 내에서 효율적으로 확산됩니다. 동일한 전환율에서 수증기를 이용한 활성화는 이산화탄소를 이용한 활성화보다 약 2~3배 더 높은 것으로 나타났습니다.
화학적 접근법은 전구체에 활성화제(NaOH, KOH, FeCl3 등)를 혼합하는 과정을 포함합니다. 이러한 활성화제는 산화제 및 탈수제 역할을 합니다. 이 접근법에서는 물리적 접근법에 비해 비교적 낮은 온도인 300~500°C에서 탄화 및 활성화가 동시에 진행됩니다. 결과적으로 열분해가 일어나 다공성 구조가 개선되고 탄소 수율이 높아집니다. 화학적 접근법의 주요 이점은 낮은 온도 요구량, 높은 미세다공성 구조, 넓은 표면적, 그리고 반응 완료 시간 단축입니다.
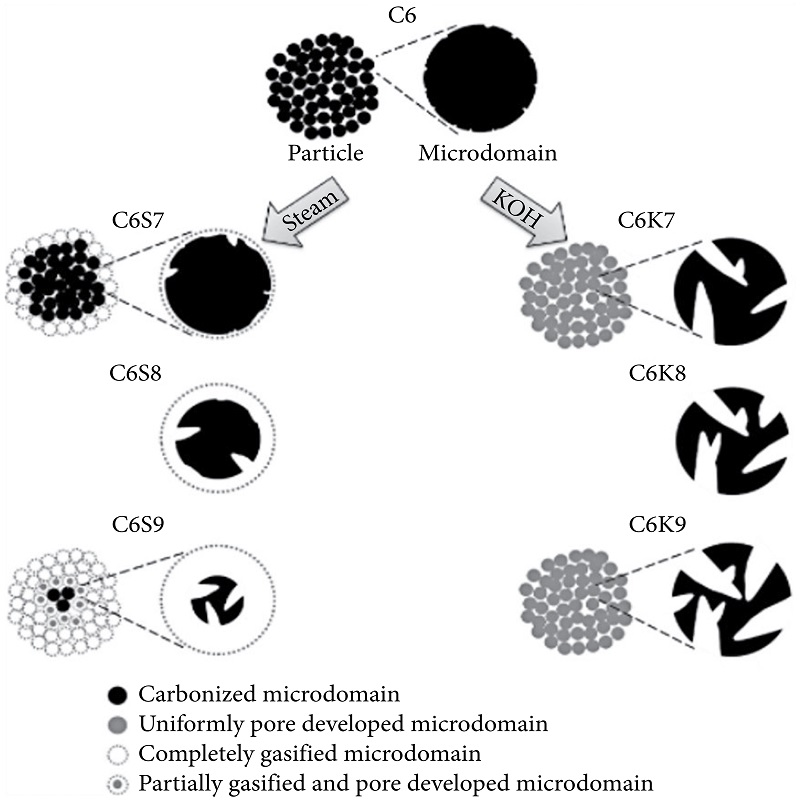
화학적 활성화 방법의 우수성은 김 등 연구진이 제안한 모델[1]을 바탕으로 설명할 수 있는데, 이 모델에 따르면 활성탄(AC)에는 미세 기공 형성에 관여하는 다양한 구형 미세 영역이 존재하며, 중간 기공은 이러한 미세 영역 사이 영역에 발달한다. 김 연구진은 실험적으로 페놀계 수지를 화학적(KOH 사용) 및 물리적(증기 사용) 활성화 방법을 이용하여 활성탄을 제조하였다(그림 1). 실험 결과, KOH 활성화 방법으로 합성된 활성탄은 증기 활성화 방법으로 합성된 활성탄(2213 m2/g)에 비해 2878 m2/g의 높은 표면적을 나타냈다. 또한, 기공 크기, 표면적, 미세 기공 부피, 평균 기공 폭 등 다른 요소들도 KOH 활성화 조건에서 증기 활성화 조건보다 우수한 것으로 나타났다.
증기 활성화(C6S9)와 KOH 활성화(C6K9)로 각각 제조된 활성탄의 차이점을 미세구조 모델을 통해 설명한다.
입자 크기와 제조 방법에 따라 활성탄은 분말형, 과립형, 비드형의 세 가지 유형으로 분류할 수 있습니다. 분말형 활성탄은 평균 직경이 0.15~0.25mm인 1mm 크기의 미세한 과립으로 구성됩니다. 과립형 활성탄은 분말형에 비해 크기가 크고 외부 표면적이 작습니다. 과립형 활성탄은 크기 비율에 따라 다양한 액상 및 기체상 응용 분야에 사용됩니다. 세 번째 유형인 비드형 활성탄은 일반적으로 석유 피치로부터 합성되며 직경은 0.35~0.8mm입니다. 높은 기계적 강도와 낮은 분진 함량으로 잘 알려져 있습니다. 구형 구조 덕분에 물 여과와 같은 유동층 응용 분야에 널리 사용됩니다.
게시 시간: 2022년 6월 18일

